本发明属于生物
技术领域:
,涉及一种多发性骨髓瘤合并慢性移植物抗宿主病小鼠模型的建立方法。
背景技术:
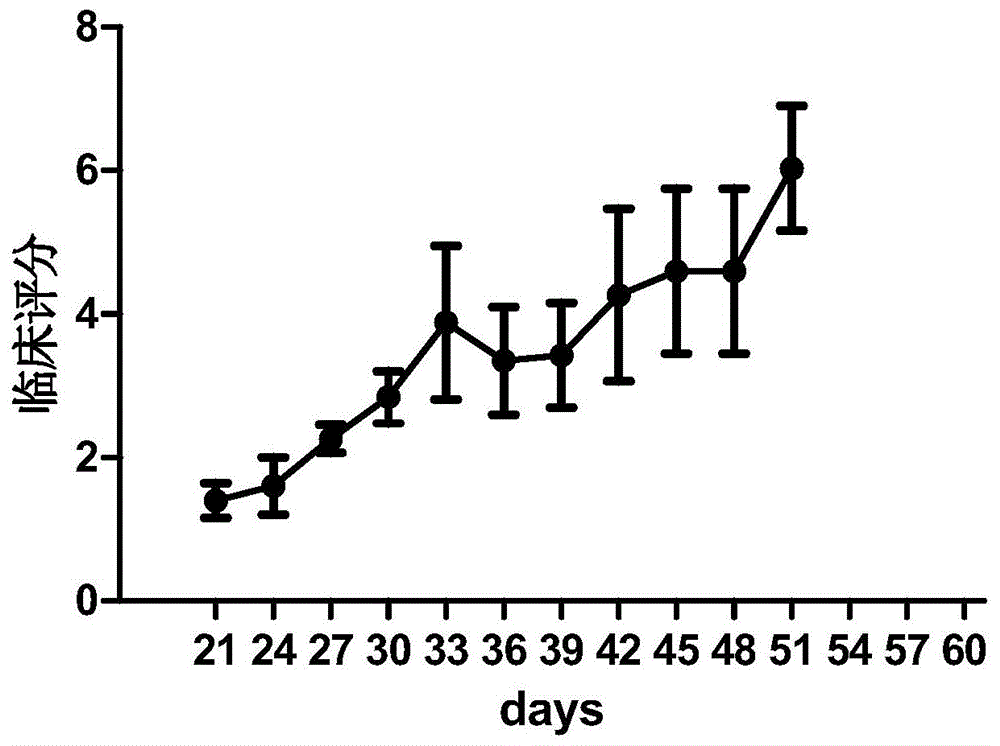
:慢性移植物抗宿主病是异基因造血干细胞移植后长期存活患者的主要并发症,不仅严重影响患者的生存质量,也是其死亡的主要原因。进一步明确cgvhd发生机制,探究gvl与gvhd的关系,研究积极有效的治疗方法,降低或减轻其发生及病程,具有重要的实际意义。因此,合并多发性骨髓瘤及cgvhd动物模型的建立,是转化医学研究的重要基础。目前大部分小鼠模型为cgvhd小鼠模型或为多发性骨髓瘤模型,尚无累及合并两种疾病的小鼠模型报道。技术实现要素:本发明的目的是提供一种小鼠多发性骨髓瘤合并慢性移植物抗宿主病模型的建立方法。为了实现上述目的,本发明采用了以下技术方案:一种小鼠多发性骨髓瘤合并cgvhd模型的建立方法,依次包括以下步骤:(1)以ncg(nod-scid-il2rg-/-)小鼠作为模型小鼠;(2)ncg(nod-scid-il2rg-/-)小鼠接受全身辐照100cgy后,将多发性骨髓瘤荧光素酶报告基因细胞株(im-9)悬液注射至ncg(nod-scid-il2rg-/-)小鼠;(3)ncg(nod-scid-il2rg-/-)小鼠接受注射后8天,将cs1car-t细胞悬液通过尾静脉注射至ncg(nod-scid-il2rg-/-)小鼠体内。优选地,所述ncg(nod-scid-il2rg-/-)小鼠为8-10周龄小鼠。具体来说,所述步骤(2)中,多发性骨髓瘤荧光素酶报告基因细胞株(im-9)悬液的制备为:24孔板内准备1×106im-9细胞,加入携带luciferase的慢病毒,感染12h后换液,3天后用嘌呤霉素筛选稳定转染的细胞,用双荧光素酶报告基因底物检测稳转细胞株内荧光素酶的活性,将稳转后的细胞株计数并用rpmi-1640重悬细胞,调整至2.5×106/ml细胞浓度备用。具体来说,携带luciferase的慢病毒的moi值为30。优选地,所述步骤(2)中,ncg(nod-scid-il2rg-/-)小鼠在接受直线加速器100cgy单次全身照射预处理后立即补充饮水,休息4-6小时后经尾静脉注射终体积为0.4ml的多发性骨髓瘤荧光素酶报告基因细胞株(im-9)悬液。具体来说,所述步骤(3)中,cs1car-t细胞悬液的制备为:正常人外周血先经过ficoll密度梯度离心法分离外周血单个核细胞(pbmcs),分选出cd3+t细胞,将分选得到的t细胞离心,并用pbs洗一次,计数,用t细胞培养基重悬为1×106/ml,种在24孔板内,1ml每孔,用humant-activatorcd3/cd28dynabeads刺激72h,经72h刺激后,收集t细胞离心,计数重悬于t细胞培养基中,加入携带抗cs1抗原的scfv慢病毒,感染12h后换液,72h检测gfp%确定转染效率,将car-t密度维持在1×106/ml左右,每2-3天进行一次半量换液。两周后,car-t细胞数扩增至足够数量,gfp阳性的细胞为转染成功的细胞,将cs1car-t细胞计数并用rpmi-1640重悬细胞,调整至12.5×106/ml细胞浓度备用。优选地,所述步骤(3)中,注射给ncg(nod-scid-il2rg-/-)小鼠的cs1car-t细胞的用量为5×106。本发明通过尾静脉回输给ncg小鼠多发性骨髓瘤细胞株(im-9)7天后,尾静脉再次回输制备好的cs1car-t细胞给ncg小鼠,建立一种多发性骨髓瘤合并cgvhd模型。其具有如下特点:(1)该模型具有模拟临床上多发性骨髓瘤患者异基因造血干细胞移植后慢性移植物抗宿主病的发生发展特点;(2)建模效率高,重复性好;(3)造模小鼠容易获得,过程简单易行;(4)皮肤等多器官同时发生典型病理改变;(5)移植后的小鼠既有多发性骨髓瘤,又合并有cgvhd,更接近人类cgvhd的病征表现,为在活体动物内进行防治人类cgvhd的研究提供新的实验平台。本发明建立具有模拟临床上多发性骨髓瘤患者异基因造血干细胞移植后慢性移植物抗宿主病的发生发展特点,可为慢性移植物抗宿主病的发生机制和诊治方法提供研究平台。本小鼠模型为实验过程中偶然的发现,本研究意为用多发性骨髓瘤细胞抗原bcma、cd138、cs1car-t治疗多发性骨髓瘤小鼠,随着cs1car-t细胞进入小鼠体内后,小鼠逐渐表现为cgvhd模型小鼠,皮肤出现溃疡、结痂、脱毛、弓背、体重下降等cgvhd临床表现,同时小鼠体内仍携带有多发性骨髓瘤细胞,在小鼠各器官he染色中发现其cgvhd病理表现。而输注针对其他抗原的car-t细胞的小鼠并不会出现cgvhd表现。本研究使用8周的ncg(nod-scid-il2rg-/-)小鼠来源方便,方法简便,小鼠症状更符合临床肿瘤患者异基因造血干细胞移植后慢性移植物抗宿主病的发生发展特点,小鼠骨髓残留肿瘤细胞,皮肤及肺部等器官cgvhd的表现典型。本方法提供了研究多发性骨髓瘤合并cgvhd的新模型,不仅为开展cgvhd与gvl相互作用的研究,还为开展肿瘤复发、cgvhd疾病防治药物研发等研究奠定基础,具有重要的实际意义。附图说明图1是d组多发性骨髓瘤+cs1car-t组小鼠的临床平分示意图(图例中每个时间点的评分以均数±标准差表示,n=5);图2是d组小鼠的临床表现,a显示皮肤脱屑、溃疡;b显示尾部肿胀、脱屑;c显示脱毛;d显示脱毛、弓背;图3是多发性骨髓瘤+cs1car-t组小鼠的肿瘤负荷流式图:a图为种瘤后第7天小鼠活体成像,小鼠全部肿瘤成功;b图为小鼠回输car-t细胞后,部分小鼠肿瘤负荷减轻;图4是多发性骨髓瘤+cs1car-t组小鼠的活体成像肿瘤负荷荧光图;图5是多发性骨髓瘤+cs1car-t组小鼠处死后分离的皮肤、肺脏、肝脏、肠道的病理组织he染色图。具体实施方式本发明结合附图和实施例作进一步的说明。本实验所用小鼠均购自南京大学模式动物研究所,在广州市中山大实验动物中心进行饲养。实施例一本例为本发明的小鼠多发性骨髓瘤合并慢性移植物抗宿主病模型的建立例,按以下步骤操作。一、小鼠准备无特定病原体(speceficpathogenfree,spf)级ncg(nod-scid-il2rg-/-)雄性小鼠(也可以采用雌性小鼠)8周龄作为模型鼠备用。本实施例的小鼠购自于南京大学模式动物研究所。将受鼠随机分为6组,每组5只;其中:a组(正常对照组):同步饲养,无干预;b组(多发性骨髓瘤对照组):全身辐照100cgy后,将多发性骨髓瘤荧光素酶报告基因(luciferase)稳转细胞株(im-9)悬液注射至ncg小鼠;8天后经尾静脉注射prmi1640培养液;c组(多发性骨髓瘤+gfp-t对照组):全身辐照100cgy后,将多发性骨髓瘤荧光素酶报告基因(luciferase)稳转细胞株(im-9)悬液注射至ncg小鼠;8天后经尾静脉注射5×106gfp-t细胞悬液;d组(多发性骨髓瘤+cs1car-t组):全身辐照100cgy后,将多发性骨髓瘤荧光素酶报告基因(luciferase)稳转细胞株(im-9)悬液注射至ncg小鼠;8天后经尾静脉注射5×106cs1car-t细胞悬液;e组(多发性骨髓瘤+bcma1car-t组):全身辐照100cgy后,将多发性骨髓瘤荧光素酶报告基因(luciferase)稳转细胞株(im-9)悬液注射至ncg小鼠;8天后经尾静脉注射5×106bcmacar-t细胞悬液;f组(多发性骨髓瘤+cd138car-t组):全身辐照100cgy后,将多发性骨髓瘤荧光素酶报告基因(luciferase)稳转细胞株(im-9)悬液注射至ncg小鼠;8天后经尾静脉注射5×106cd138car-t细胞悬液;二、根据以上分组,采用下述步骤进行移植实验操作:1、种瘤。种瘤当日(0d),对b、c、d、e、f组受鼠接受直线加速器100cgy单次全身照射预处理。照射后立即补充饮水,休息4~6小时后经尾静脉注射终体积为0.4ml的移植细胞悬液。所述移植细胞悬液指多发性骨髓瘤荧光素酶报告基因(luciferase)稳转细胞株(im-9)悬液。b组:小鼠中每只从尾静脉输注多发性骨髓瘤荧光素酶报告基因(luciferase)稳转细胞株(im-9)悬液,细胞量为1×10^6;c组:小鼠中每只从尾静脉输注多发性骨髓瘤荧光素酶报告基因(luciferase)稳转细胞株(im-9)悬液悬液0.4ml,细胞量为1×10^6;d组:小鼠中每只从尾静脉输注多发性骨髓瘤荧光素酶报告基因(luciferase)稳转细胞株(im-9)悬液悬液0.4ml,细胞量为1×10^6;e组:小鼠中每只从尾静脉输注多发性骨髓瘤荧光素酶报告基因(luciferase)稳转细胞株(im-9)悬液悬液0.4ml,细胞量为1×10^6;f组:小鼠中每只从尾静脉输注多发性骨髓瘤荧光素酶报告基因(luciferase)稳转细胞株(im-9)悬液悬液0.4ml,细胞量为1×10^6;其中,多发性骨髓瘤荧光素酶报告基因(luciferase)稳转细胞株(im-9)悬液的制备:24孔板内准备1×106im-9细胞,加入携带luciferase的慢病毒(moi值为30),感染12h后换液(t细胞培养基),3天后用嘌呤霉素筛选稳定转染的细胞,最终用双荧光素酶报告基因底物检测稳转细胞株内荧光素酶的活性。将稳转后的细胞株计数并用rpmi-1640重悬细胞,调整至2.5×106/ml细胞浓度备用。2、回输car-t细胞悬液。种瘤后+8d,小鼠活体成像明确小鼠种瘤成功,尾静脉回输car-t细胞。b组回输0.4mlprmi1640培养液,c组经尾静脉回输5×106gfp-t细胞悬液,d组经尾静脉注射5×106cs1car-t细胞悬液,e组经尾静脉注射5×106bcmacar-t细胞悬液,f组经尾静脉注射5×106cd138car-t细胞悬液。其中,cs1car-t细胞悬液的制备如下:正常人外周血先经过ficoll密度梯度离心法分离外周血单个核细胞(pbmcs),参照美天旎公司pantisolationkit的说明书分选出t细胞,将分选得到的t细胞离心,并用pbs洗一次,计数,用t细胞培养基(rpmi-1640+10%fbs+300u/mlil-2+1%p/s)重悬为1×106/ml,种在24孔板内,1ml每孔,用humant-activatorcd3/cd28dynabeads刺激72h。经72h刺激后,收集t细胞离心,计数重悬于t细胞培养基中,加入携带抗cs1基因的慢病毒(moi值为30),感染12h后换液,3天检测gfp%确定转染效率,将car-t密度维持在1×106/ml左右,每2-3天进行一次半量换液。两周后,car-t细胞数可扩增100倍,gfp阳性的细胞为转染成功的细胞,将cs1car-t细胞计数并用rpmi-1640重悬细胞,调整至12.5×106/ml细胞浓度备用。每天观察小鼠一般状态,包括体重、皮疹、脱毛、结痂、弓背、腹泻等,尾静脉回输cs1car-t细胞14天后每3天进行一次临床评分,标准参见表1;濒死小鼠处死取材,其存活时间记至死次日。表1慢性gvhd的临床评分标准得分0分1分2分3分脱毛无<1cm21~2cm2>2cm2体重减轻无或减轻≤2%2%~8%≥8%弓背体态无不影响运动影响运动注:(a)耳朵、尾巴、脚掌每处脱皮或结痂记0.3分,皮肤临床表现最低得0分,最高得3.9分。(b)皮肤得分超过0.6分视为发生gvhd;即使症状消退、小鼠自然死亡或人为因素造成死亡也视为发生gvhd;小鼠无症状死亡视为无gvhd。观察记录表明:a组小鼠正常存活至实验终点;b、c组小鼠中位存活25天,30天内全部死亡;d、f组小鼠中位存活35天,部分小鼠存活至实验终点,e组小鼠中位存活40天,部分小鼠存活至实验终点。以上记录b、c、d、e、f组均种瘤成功,d组予cs1car-t治疗后,表现为cgvhd表现,可延长小鼠生存时间,其他组小鼠不出现cgvhd表现。实施例二本例为多发性骨髓瘤合并cgvhd组小鼠肿瘤负荷活体成像的检测例。1、对于im-9细胞,由于表达luciferase,可以通过底物进行成像,检测im-9细胞残留以及生长状况;2、通过腹腔注射底物d-luciferin200ul(15mg/ml),计时5分钟后,放入体内成像仪附带的麻醉室内,同时异氟烷进行麻醉;3、将麻醉好的小鼠放入成像仪内进行成像,通过自动曝光模式模式进行成像(即曝光时间会根据信号强弱自动调节);4、成像结束后,将小鼠放回笼子内饲养;5、数据分析。如图3所示:a图为种瘤后第7天小鼠活体成像,小鼠全部肿瘤成功;b图为小鼠回输car-t细胞后,部分小鼠肿瘤负荷减轻。实施例三本例为多发性骨髓瘤合并cgvhd小鼠肿瘤负荷流式细胞术的检测例。1、对于im-9细胞株,由于其表达cs1抗原,可以通过流式细胞术检测外周血中cs1抗原的表达量,检测im-9细胞的残留情况;2、对多发性骨髓瘤+cs1car-t组小鼠尾静脉采血;3、将小鼠外周血进行anti-humancs1染色30分钟,30分钟后用红细胞裂解液500ul加入流式管中,裂解10分钟,加入3mlpbs洗涤,300g离心5min,再次用pbs洗涤一次,加入200ulpbs备用。4、上机检测cs1抗原表达量,分析数据。如图4所示:d组小鼠体内cs1抗体表达,图中cs1进一步证明小鼠肿瘤负荷,体内残留多发性骨髓瘤肿瘤细胞。实施例四本例为多发性骨髓瘤合并cgvhd组小鼠的临床及病理检测例。一、对d组小鼠进行慢性gvhd的临床评分,其评分标准如表1所示:表1慢性gvhd的临床评分标准得分0分1分2分3分脱毛无<1cm21~2cm2>2cm2体重减轻无或减轻≤2%2%~8%≥8%弓背体态无不影响运动影响运动注:(a)耳朵、尾巴、脚掌每处脱皮或结痂记0.3分,皮肤临床表现最低得0分,最高得3.9分。(b)皮肤得分超过0.6分视为发生gvhd;即使症状消退、小鼠自然死亡或人为因素造成死亡也视为发生gvhd;小鼠无症状死亡视为无gvhd。濒死小鼠处死取材,其存活时间记至处死次日。图1为d组小鼠的临床评分示意图。(图例中每个时间点的评分以均数±标准差表示,n=5)图2为d组小鼠的临床表现,a显示皮肤脱屑、溃疡;b显示尾部肿胀、脱屑;c显示脱毛;d显示脱毛、弓背。二、对+60天的d组小鼠进行慢性gvhd的病理检测,病理评分标准如表2所示:表2慢性gvhd的病理评分标准注:(l)得分超过2视为发生gvhd。取c组及d组受鼠处死后进行检测,按以下步骤进行:1、固定:取各脏器组织切成小块,10%中性福尔马林溶液内固定24小时;2、以下程序在shandon全自动密闭脱水机中完成:2.1把固定好的组织标本分别在80%乙醇50min,90%乙醇50min,95%乙醇ⅰⅱ各40min,100%乙醇ⅰⅱ各40min;2.2将脱水后标本分别在二甲苯ⅰ、ⅱ、ⅲ中放置30min;2.3低熔点石蜡ⅰ、ⅱ、ⅲ中放置各25min(温度设置为62摄氏度);2.4高熔点石蜡ⅰ缸25min(温度设置为64摄氏度);3、组织处理程序结束后,取出标本,置于包埋机的蜡槽中,进行包埋(温度设置为62摄氏度);4、切片:在切片机上切下4μm切片,漂在干净的水面上,在50-57摄氏度温水中展开,再将组织切片捞起;在70摄氏度烤箱中烘烤15-20min;5、从烤箱中取出切片,室温稍冷却,将切片放到染色机上进行全自动he染色,染色程序如下:二甲苯ⅰ、ⅱ、ⅲ中放置各7min,100%乙醇ⅰⅱ、95%乙醇ⅰⅱ、80%乙醇、蒸馏水各1min;。苏木精染液中15分钟,水洗,0.5%盐酸酒精10s;2%碳酸锂水溶液1min;流水冲洗10min,80%乙醇、95%乙醇ⅰⅱ,80%乙醇,100%乙醇ⅰⅱⅲ、二甲苯ⅰ、ⅱ各1min;6、取出切片,将切片挂上shandon封片机进行封片。7、光学显微镜下观察he染色组织切片,病理结果描述:光学显微镜下观察he染色组织切片发现小鼠肺脏表现为阻塞性细支气管炎,细支气管内大量炎性细胞浸润,阻塞细支气管腔,管壁平滑肌层被破坏,及肺实变;尾皮肤溃疡,真皮层大量胶原沉积,炎症细胞浸润;肝细胞颗粒变性、水肿,汇管区少量炎症细胞浸润;肠道局部炎性细胞浸润;图4为多发性骨髓瘤+cs1car-t组小鼠+60天处死后分离的肺、皮肤、肠道和肝脏的病理活检he染色图。结果显示:多发性骨髓瘤+cs1car-t组小鼠肺部呈阻塞性细支气管炎,细支气管内大量炎性细胞浸润,阻塞细支气管腔,管壁平滑肌层被破坏(×100,×200);皮肤真皮层胶原沉积,炎症细胞浸润(×100,×200);肠道局部炎症细胞浸润(×100,×200);肝脏炎症细胞浸润(×100,×200)。检测结果表明,多发性骨髓瘤+cs1car-t组小鼠在肺脏、皮肤、肠道和肝脏均表现出cgvhd症状,与人类异基因移植后所表现的cgvhd症状非常相似。当前第1页1 2 3
想要进行版权登记、专利购买,商标买卖的相关服务,就来大鱼知产进行详细了解,更多专业知识与专业人士将为您服务到底,想要更快的了解版权登记、专利购买,商标买卖相关问题,我们来帮您。热线电话:13018202357,客服微信(13018202357)
以上就是大鱼知产平台为各位讲解的有关
一种多发性骨髓瘤合并慢性移植物抗宿主病小鼠模型的建立方法与流程
的介绍,相信各位对于商标申请注销的流程中需要注意和了解的事项,可以有一定的认识,若各位还想要了解更多有关专利行业资讯
的问题,欢迎到大鱼知产平台进行相关问题咨询吧!




